Ferroïne
La ferroïne est un composé chimique de formule [Fe(o-phen)3]SO4, où o-phen représente la 1,10-phénantroline, un ligand bidentate. Le terme ferroïne est assez vague et comprend également des sels d'autres anions que le sulfate SO42− tels que le chlorure Cl−.
| Ferroïne | |
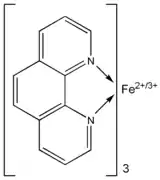 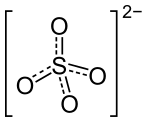 Structure de la ferroïne |
|
| Identification | |
|---|---|
| Synonymes |
sulfate de tris(1,10-phénanthroline)fer(II) |
| No CAS | |
| No ECHA | 100.035.145 |
| No CE | 238-676-6 |
| PubChem | 84567 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C36H24FeN6O4S |
| Masse molaire[1] | 692,524 ± 0,04 g/mol C 62,44 %, H 3,49 %, Fe 8,06 %, N 12,14 %, O 9,24 %, S 4,63 %, |
| Précautions | |
| SGH[2] | |
 |
|
| Unités du SI et CNTP, sauf indication contraire. | |
Ce complexe est utilisé comme indicateur coloré en chimie analytique. L'ion [Fe(o-phen)3]2+ est la partie active de la molécule ; il s'agit d'un chromophore qui peut être oxydé en son dérivé ferrique [Fe(o-phen)3]3+ avec un potentiel d'oxydoréduction de +1,06 V à 1 mol·L-1 dans l'acide sulfurique H2SO4.
Le sulfate de ferroïne peut être préparé en combinant de la phénanthroline avec du sulfate de fer(II) FeSO4 dans l'eau :
- 3 (1,10-phénantroline) + Fe2+ → [Fe(o-phen)3]2+, l'anion SO42− étant présent des deux côtés de la réaction.
La couleur rouge intense de ce complexe ferreux provient du transfert de charge du métal vers le ligand[réf. souhaitée] ; la forme oxydée, avec le cation ferrique Fe3+, est de couleur bleue.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Portail de la chimie