Dichlorure de xénon
Le dichlorure de xénon, de formule XeCl2, est un composé du chlore et du xénon. Seul chlorure de xénon ![]() connu pour être stable, il peut être préparé par des décharges micro-ondes dans un mélange de xénon et de chlore gazeux, et isolé par un piège à condensats.
connu pour être stable, il peut être préparé par des décharges micro-ondes dans un mélange de xénon et de chlore gazeux, et isolé par un piège à condensats.
| Dichlorure de xénon | |
| |
| Identification | |
|---|---|
| Nom UICPA | Dichloroxenon |
| No CAS | |
| Propriétés chimiques | |
| Formule | XeCl2 |
| Masse molaire[1] | 202,199 ± 0,01 g/mol Cl 35,07 %, Xe 64,93 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
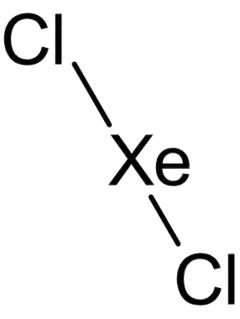
La molécule XeCl2 est généralement considérée comme constituée d'un atome de xénon lié séparément à deux atomes de chlore, mais il s'agit peut-être d'une molécule de van der Waals Xe-Cl2 (un atome de xénon lié à une molécule de dichlore par une liaison de van der Waals)[2].
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Xenon dichloride » (voir la liste des auteurs).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Davide M. Proserpio, Roald Hoffmann et Kenneth C. Janda, « The xenon-chlorine conundrum: van der Waals complex or linear molecule? », Journal of the American Chemical Society, vol. 113, no 19, , p. 7184-7189 (DOI 10.1021/ja00019a014).
- Portail de la chimie
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons – Attribution – Partage à l’identique. Des conditions supplémentaires peuvent s’appliquer aux fichiers multimédias.