Acide phloroglucinique
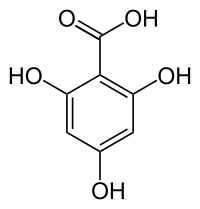
L'acide phloroglucinique ou acide 2,4,6-trihydroxybenzoïque est un composé organique aromatique dérivé de l'acide benzoïque et du phloroglucinol ((1,3,5-trihydroxybenzène). Il est constitué d'un cycle benzénique substitué par un groupe carboxyle et par trois groupes hydroxyle, aux position 2, 4 et 6 , et est donc l'un des six isomères de l'acide trihydroxybenzoïque.
| Acide phloroglucinique | |
| |
| Identification | |
|---|---|
| Nom systématique | acide 2,4,6-trihydroxybenzoïque |
| No CAS | |
| No ECHA | 100.001.334 |
| No CE | 201-467-5 |
| PubChem | 66520 |
| SMILES | |
| InChI | |
| Apparence | poudre beige[1] |
| Propriétés chimiques | |
| Formule | C7H6O5 [Isomères] |
| Masse molaire[2] | 170,119 5 ± 0,007 5 g/mol C 49,42 %, H 3,55 %, O 47,02 %, |
| pKa | 1,68 à 25 °C[3] |
| Propriétés physiques | |
| T° fusion | 100 °C (décomposiion)[4] |
| Solubilité | légèrement soluble dans l'eau, soluble dans l'éthanol, très soluble dans l'éther, insoluble dans le benzène[4] |
| Précautions | |
| SGH[1] | |
 Attention |
|
| Écotoxicologie | |
| DL50 | > 800 mg·kg-1 (souris, i.p.)[5] |
| Unités du SI et CNTP, sauf indication contraire. | |
L'acide phloroglucinique est notamment produit par Pseudomonas fluorescens[6].
Acinetobacter calcoaceticus lorsqu'elle se développe sur les cultures absorbe la (+)-catéchine comme sa seule source de carbone, la dégrade en acide phloroglucinecarboxylique et l'excrète[7],[8].
L'acide phloroglucinique a également été détecté dans le vin[9].
Notes et références
- Fiche Sigma-Aldrich du composé 2,4,6-trihydroxybenzoic acid, consultée le 21 septembre 2020..
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (de) D'Ans-Lax, Taschenbuch für Chemiker und Physiker, vol. 1, Springer, , 3e éd. (lire en ligne)
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 90e éd., 2804 p. (ISBN 9781420090840, présentation en ligne), p. 502
- Journal of Pharmacology and Experimental Therapeutics. Vol. 196, p478, 1976.
- Jihane Achkar, Mo Xian, Huimin Zhao and J. W. Frost, « Biosynthesis of Phloroglucinol », J. Am. Chem. Soc., vol. 127, , p. 5332-5333 (DOI 10.1021/ja042340g)
- Alexandr Nemec, Lenka Krizova, Martina Maixnerova, Ondrej Sedo, Sylvain Brisse et Paul G. Higgins, « Acinetobacter seifertii sp. nov., a member of the Acinetobacter calcoaceticus–Acinetobacter baumannii complex isolated from human clinical specimens », International Journal of Systematic and Evolutionary Microbiology, vol. 65, no Pt 3, , p. 934–942 (PMID 25563912, DOI 10.1099/ijs.0.000043)
- M. Arunachalam, N. Mohan, R. Sugadev, P. Chellappan, A. Mahadevan, « Degradation of (+)-catechin by Acinetobacter calcoaceticus MTC 127 », Biochimica et Biophysica Acta, vol. 1621, no 3, (PMID 12787923, DOI 10.1016/S0304-4165(03)00077-1)
- C. García Barroso, R. Cela Torrijos and J. A. Pérez-Bustamante, « HPLC separation of benzoic and hydroxycinnamic acids in wines », Chromatographia, vol. 17, no 5, , p. 249–252 (DOI 10.1007/BF02263033)
- Portail de la chimie
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons – Attribution – Partage à l’identique. Des conditions supplémentaires peuvent s’appliquer aux fichiers multimédias.