2,4,5-Trichlorophénol
Le 2,4,5-trichlorophénol est l'un des isomères du trichlorophénol.
| 2,4,5-Trichlorophénol | |
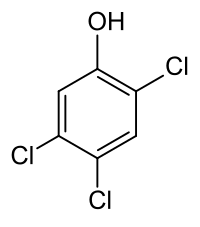
| |
| Identification | |
|---|---|
| Nom UICPA | 2,4,5-Trichlorophénol |
| Synonymes |
1-Hydroxy-2,4,5-trichlorbenzène |
| No CAS | |
| No ECHA | 100.002.244 |
| No CE | 202-467-8 |
| PubChem | 7271 |
| Apparence | aiguilles incolores à blanches, odeur similaire au phénol[1] |
| Propriétés chimiques | |
| Formule | C6H3Cl3O [Isomères] |
| Masse molaire[2] | 197,446 ± 0,011 g/mol C 36,5 %, H 1,53 %, Cl 53,87 %, O 8,1 %, |
| Propriétés physiques | |
| T° fusion | 67 °C[1] |
| T° ébullition | 253 °C[1] |
| Solubilité | 1 190 mg·l-1 (eau, 20 °C)[1] |
| Masse volumique | 1,678 g·cm-3 (25 °C)[1] |
| Point d’éclair | 133 °C (coupelle fermée)[1] |
| Précautions | |
| SGH[1] | |
  |
|
| Transport[1] | |
| Écotoxicologie | |
| DL50 | 820 mg·kg-1[3] |
| LogP | 3,72[1] |
| Unités du SI et CNTP, sauf indication contraire. | |
Propriétés
D'après la base de données GESTIS[1].
Le 2,4,5-trichlorophénol est un solide cristallin incolore avec une odeur similaire au phénol. Il est peu soluble dans l'eau (1,2 g·l-1), mais soluble dans les solvants organiques apolaires (hydrocarbures). Il tend à se décomposer, de façon explosive, quand il est chauffé, produisant des composés toxiques organochlorés, dibenzofuranes et dibenzo-p-dioxine. Il réagit de façon dangereuse en présence d'ammoniac, d'oxydants et d'eau.
Utilisation
Le 2,4,5-trichlorophénol est utilisé pour la préparation d'hexachlorophène, d'acide 2,4,5-trichlorophénoxyacétique et autres dérivés[1].
Notes et références
- Entrée « 2,4,5-Trichlorophenol » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 5 juin 2013 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Federation Proceedings, Federation of American Societies for Experimental Biology, vol. 2, p. 76, 1943.
- Portail de la chimie
Cet article est issu de Wikipedia. Le texte est sous licence Creative Commons – Attribution – Partage à l’identique. Des conditions supplémentaires peuvent s’appliquer aux fichiers multimédias.
